Schematische Diagramme des elektrochemischen Gassensors und der chemischen Reaktionen
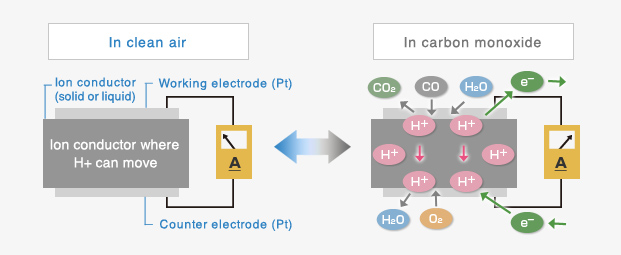
Der elektrochemische Gassensor Figaro sind amperometrische Brennstoffzellen mit zwei Elektroden. Die Grundkomponenten von zwei Elektrodengassensoren sind eine Arbeitselektrode, eine Gegenelektrode und ein Ionenleiter dazwischen. Wenn toxisches Gas wie Kohlenmonoxid (CO) mit der Arbeitselektrode in Kontakt kommt, tritt an der Arbeitselektrode eine Oxidation von CO-Gas durch chemische Reaktion mit Wassermolekülen in der Luft auf (siehe Gleichung 1).
CO + H2O → CO2+ 2H+ + 2e- …(1)
Wenn die Arbeitselektrode und die Gegenelektrode durch einen Kurzschluss verbunden werden, können Protonen (H +), die an der Arbeitselektrode erzeugt werden, durch den Ionenleiter zur Gegenelektrode fließen. Zusätzlich bewegen sich erzeugte Elektronen durch die externe Verdrahtung zur Gegenelektrode. An der Gegenelektrode findet eine Reaktion mit Sauerstoff in der Luft statt (siehe Gleichung 2).
(1/2) O2 + 2H + + 2e- → H2O …(2)
Die Gesamtreaktion ist in Gleichung 3 dargestellt. Der elektrochemische Gassensor vom Typ Figaro arbeitet wie eine Batterie, wobei Gas das aktive Material für diese Gesamtbatteriereaktion ist.
CO + (1/2) O2 → CO2 …(3)
Durch Messung des Stroms zwischen der Arbeitselektrode und der Gegenelektrode kann diese elektrochemische Zelle als Gassensor genutzt werden.
Theoretische Gleichung zur CO-Detektion
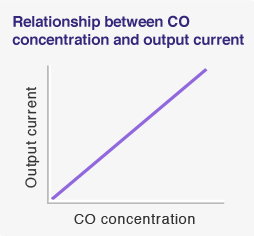
Um den Ausgangsstrom des Sensors zu messen, muss er an einen externen Stromkreis angeschlossen werden. Durch die Steuerung des zur Arbeitselektrode strömenden Gases mit Diffusionsfilm ist der über den externen Stromkreis fließende Ausgangsstrom proportional zur Gaskonzentration (siehe Gleichung 4 und die Tabelle rechts). Die lineare Beziehung der Gaskonzentration zur Sensorleistung macht diese Technologie ideal für Gassensoranwendungen.
Ich = F × (A / σ) × D × C × n …(4)
wo:
I: Sensorausgang
F: Faraday-Konstante
A: Oberfläche des Diffusionsfilms
σ: Dicke des Diffusionsfilms
D: Gasdiffusionskoeffizient
C: Gaskonzentration
n: Anzahl der Reaktionselektronen
Eigenschaften
Das Oxidationspotential von CO-Gas (wie in Gleichung 1 ausgedrückt) ist niedriger als das Oxidationspotential der Elektrode (2H + + 2e- ⇔ H2), d. H. Die Oxidation von CO hat ein weniger edles Potential als die Desoxidation. Da diese Reaktion leicht abläuft, wird im Gegensatz zu Sensoren mit drei Elektroden keine externe Energie benötigt, um die chemische Reaktion des Sensors zu stimulieren. Als Ergebnis bietet dieser Zwei-Elektroden-Sensor überlegene Eigenschaften für Störfestigkeit, Wiederholbarkeit und Stromverbrauch.